“群英荟——淋巴瘤诊疗研究解读系列会”是为中青年血液科医生打造的专属学术交流平台,通过精读淋巴瘤领域有影响力的研究文献、讨论淋巴瘤诊疗热点话题,共同探索并总结淋巴瘤的优化诊疗策略,以提升中国淋巴瘤患者的生存率。
本期由中国人民解放军总医院黄文荣教授和广西医科大学第一附属医院彭志刚教授担任大会主席,广西医科大学第一附属医院李静教授、河北医科大学第四医院黄晨教授为大家解读侵袭性淋巴瘤领域的前沿文献,并邀请中国医学科学院血液病医院易树华教授、郑州大学第一附属医院王新华教授、赤峰市医院孙莹教授和哈尔滨血液病肿瘤研究所赵东陆教授参与交流讨论,现将本期会议精彩内容整理如下。

文献精读(一)
DLBCL治疗新药辈出,临床治疗如何排兵布阵?
李静教授分享了Journal of Hematology & Oncology发表的一篇题目为“New agents and regimens for diffuse large B cell lymphoma(弥漫性大B细胞淋巴瘤[DLBCL]的新型药物和治疗方案)”[1]的文章。该综述总结了DLBCL中目前极具前景的治疗方法的最新进展,并根据新的遗传信息分类系统指导个体化治疗。
DLBCL治疗亟待新的探索
近年来,为了改善非生发中心B细胞样(non-GCB)或活化B细胞样(ABC)亚型DLBCL患者的预后,一些随机临床研究在R-CHOP模式中添加新的靶向药物(R-CHOP+X模式),如硼替佐米、来那度胺或伊布替尼。然而,这些靶向药物在研究中未能带来显著益处。此外,在一项III期随机研究(CALGB 50303)中,DA-EPOCH-R也未能显示DLBCL患者的生存结局改善。标准的R-CHOP方案能够治愈三分之二的DLBCL患者,其余患者由于对R-CHOP的耐药性而出现难治性或复发性疾病,预后较差。
* R-CHOP:利妥昔单抗、环磷酰胺、多柔比星、长春新碱、泼尼松;DA-EPOCH-R:剂量调整的依托泊苷、泼尼松、长春新碱、环磷酰胺、多柔比星和利妥昔单抗
新药异军突起,带来更多治疗新选择
近年来,维泊妥珠单抗(Polatuzumab Vedotin,简称Pola)、塞利尼索、tafasitamab、靶向CD19 CAR-T获得FDA批准用于DLBCL治疗,多种靶向免疫检查点、肿瘤微环境、分子信号通路、表观遗传突变以及细胞免疫治疗的治疗方法共同构成了DLBCL治疗的新格局。
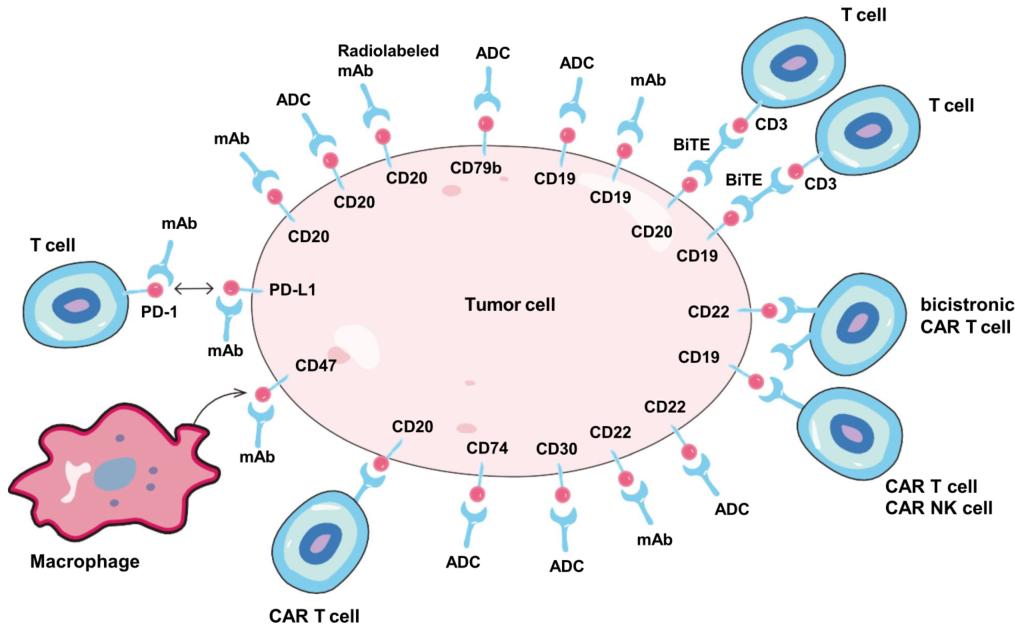
ADC:2019年,FDA批准靶向CD79b的ADC药物Pola联合苯达莫司汀、利妥昔单抗(Pola-BR)用于至少经两线治疗的复发/难治性(R/R)DLBCL患者。在一项多中心Ib/II期研究中,Pola联合R-CHP或G-CHP治疗初治DLBCL患者的疗效良好,总缓解率(ORR)和完全缓解(CR)率分别达到89%和77%;1.8 mg/kg剂量的Pola显示出总体可接受的安全性,38%(25/66)患者发生1-2级周围神经病变。鉴于Pola显著的疗效和可管理的安全性,Pola联合其他药物(包括来那度胺、维奈克拉和奥妥珠单抗)应用于R/R DLBCL的多项研究正如火如荼地进行。
* R-CHP:利妥昔单抗、环磷酰胺、多柔比星、泼尼松;G-CHP:奥妥珠单抗、环磷酰胺、多柔比星、泼尼松
CAR-T疗法:Axi-cel、liso-cel和tisa-cel在靶向CD19 CAR-T细胞治疗中已被证明有效。在ZUMA-1研究中,既往至少接受三种治疗方案的难治性侵袭性B细胞非霍奇金淋巴瘤(NHL)患者接受靶向CD19 CAR-T治疗的ORR为83%,CR率达到54%,且总生存期(OS)显著改善。另有研究显示CAR-T细胞联合PD-1/PD-L1抑制剂治疗R/R DLBCL似乎可行。靶向CD19和CD20/CD22的双靶点CAR-T、通用型CAR-T在B细胞淋巴瘤中的探索充满希望,在不久的将来可以成为高危患者二线甚至一线治疗方案。
BiTE:贝林妥欧单抗是一种CD19/CD3 BiTE,已被FDA批准用于治疗R/R B细胞急性淋巴细胞白血病的治疗。一项II期研究表明贝林妥欧单抗单药治疗R/R侵袭性B细胞淋巴瘤有效,可以桥接自体造血干细胞移植(ASCT)。
免疫调节药物:来那度胺作为一种免疫调节剂,单药或联合挽救性化疗(如R-ICE和R-ESHAP)已被证明对R/R DLBCL有效。无化疗方案R2(利妥昔单抗+来那度胺)在老年R/R DLBCL患者中的疗效也得到证实,35%的患者实现了持久CR,这使得R2成为不符合ASCT条件的老年患者的治疗选择。此外,来那度胺具有穿透血脑屏障的能力,被证实对原发性中枢神经系统淋巴瘤(PCNSL)具有较高的活性。因此,在免疫化疗中加入来那度胺可能会降低CNS复发的风险,这有待于未来的验证。
* R-ICE:利妥昔单抗、异环磷酰胺、依托泊苷、卡铂;R-ESHAP:利妥昔单抗、依托泊苷、地塞米松、阿糖胞苷、顺铂
展望
虽然近年来一些新的分子分型系统出现,但约有一半的患者无法被划分为特定的亚型,这些分子亚型在常规临床实践中应用还需要更多研究进行探索。治愈DLBCL还有很长的路要走,相信在详细的遗传信息的指导下,新药物和传统药物的最佳组合将出现,以促进DLBCL患者的精准治疗。
专家热点讨论
在李静教授的精彩解读后,多位专家就各类新型药物在DLBCL中的应用前景展开讨论。彭志刚教授认为,在DLBCL治疗中,首先需要对患者进行预后评估与危险分层,以指导个体化治疗。王新华教授提出,目前CAR-T的临床应用主要受限于其较高的售价,相信随着市场竞争的推动和更多临床研究的开展,CAR-T的可及性将逐渐提高。易树华教授认为,目前的研究数据显示,CAR-T以及Pola、双特异性抗体Glofitamab和Mosunetuzumab等新型免疫治疗药物均表现不俗,今后或将在DLBCL治疗方案的排兵布阵上占据主导地位。针对CAR-T耐药的患者,未来可通过设计更好的靶点或跟Pola等新药联合应用以提高疗效。
文献精读(二)
BR方案一线治疗适合移植的MCL与其他常见化疗方案相当
黄晨教授分享了Blood Advances发表的一篇题目为“Bendamustine or high‐dose cytarabine‐based induction with rituximab in transplant‐eligible mantle cell lymphoma(BR或R-DHAP方案诱导适合移植套细胞淋巴瘤[MCL]的回顾性分析)”[2]的文章。该研究证实了BR方案序贯ASCT联合利妥昔单抗维持治疗(MR)是一种可行且有效的一线治疗方法,其结果与R-CHOP或R-DHAP方案联合ASCT相当。
* BR:利妥昔单抗、苯达莫司汀;R-DHAP:利妥昔单抗、顺铂、阿糖胞苷、地塞米松
研究背景
年轻MCL患者的标准一线治疗方案是利妥昔单抗联合细胞毒药物化疗序贯ASCT,再联合MR。研究表明,在符合移植条件的患者中,BR方案无论是缓解率、ASCT成功率还是治疗结果均与R-CHOP相近,且毒性更小。然而,BR从未与R-CHOP或R-DHAP作为ASCT前的诱导治疗进行疗效比较。本研究探讨在符合移植条件MCL患者的一线治疗中,BR和R-CHOP、R-DHAP方案的治疗结果差异。
研究方法
该研究对一线接受BR治疗序贯ASCT、MR的97例18-65岁的II-IV期MCL患者和欧洲MCL Younger研究R-CHOP/R-DHAP+ASCT组的232例MCL患者进行回顾性分析。两组患者的Ann Arbor分期、乳酸脱氢酶、MCL国际预后指数(MIPI)、母细胞型/多形性细胞形态和MCL35评分基线相近。但是BR组有更高比例的不良预后特征,包括较差的体能状态和Ki67升高。主要终点为两组间PFS的风险比(HR),次要终点包括缓解率等。
表1 患者的基线特征
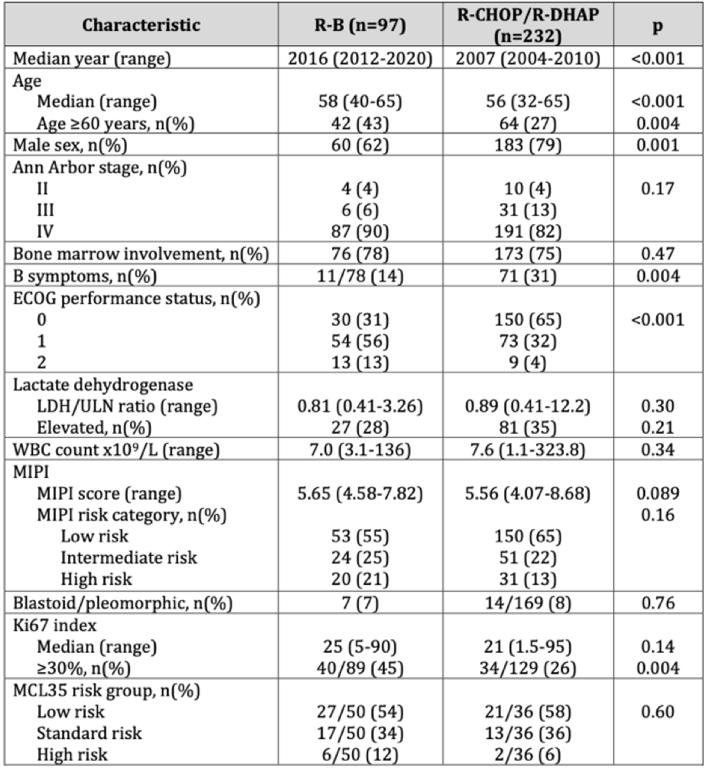
研究结果
BR组与R-CHOP/R-DHAP组的PFS,无论是校正前(HR 0.87[95%CI 0.53-1.41],P=0.56)还是校正后(HR 0.79[95%CI 0.45-1.37],P=0.40),均无统计学差异。
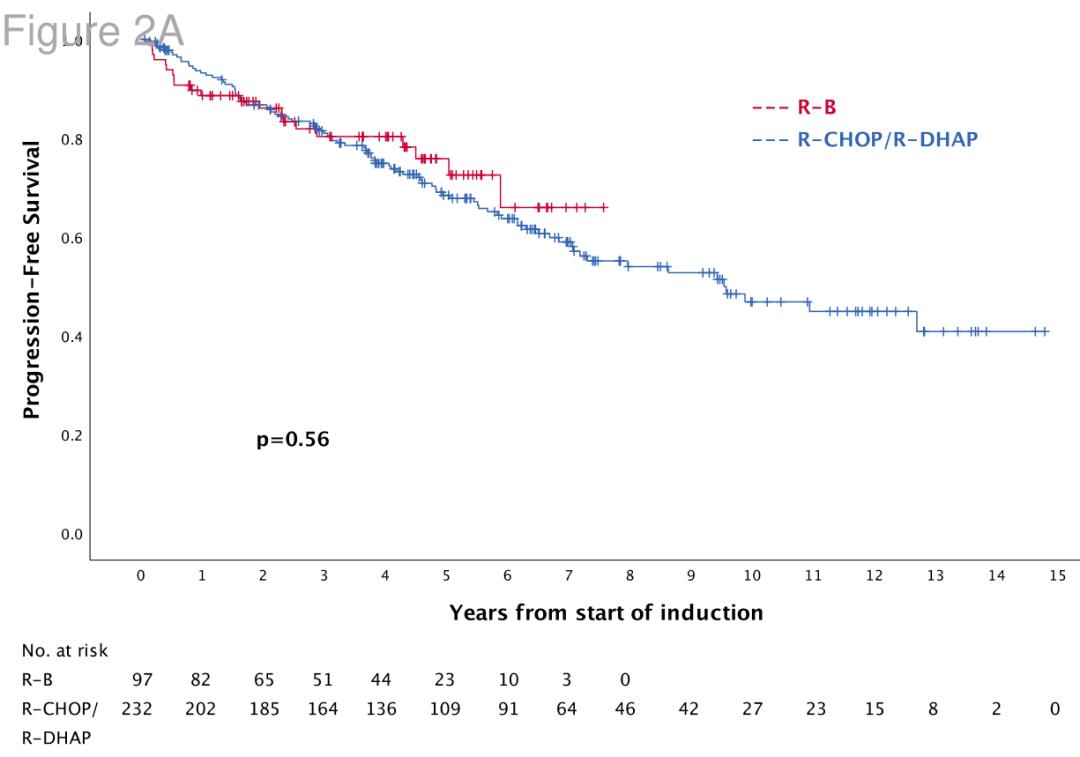
两组的次要终点疗效相当(ORR,90% vs 94%;CR率,54% vs 54%),在治疗后达到CR或部分缓解(PR)患者中,BR组干细胞动员不足的发生率更低(0 vs 8.5%)。两组诱导治疗后成功进行ASCT的患者比例分别为77%、78%;BR接受MR的患者比例显著更多(78% vs 2%,P<0.001),如表2。
表2 缓解率、诱导治疗后的序贯治疗及结果
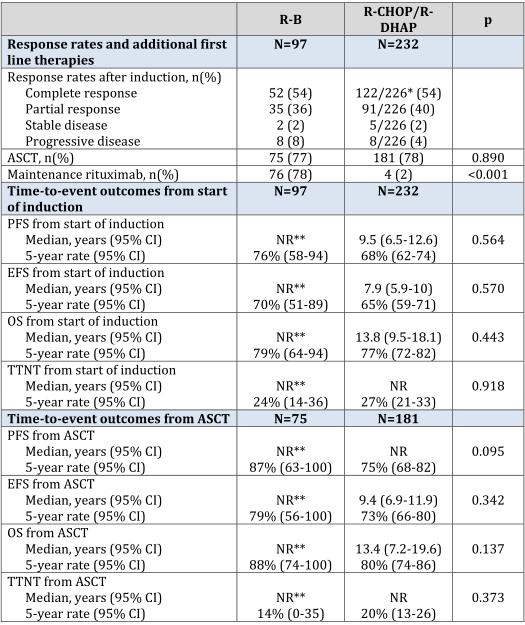
与R-CHOP/R-DHAP组相比,尽管BR组无详细的毒性数据,但研究显示BR方案可在门诊安全使用,毒性更小。
研究结论
BR序贯ASCT联合MR可能是符合移植条件的较年轻MCL患者一种合理的一线治疗方案。与R-CHOP/R-DHAP方案相比,BR方案可在门诊安全使用,毒性更小。BR与新药联合应用将成为MCL治疗的未来趋势。
专家热点讨论
在黄晨教授的精彩解读后,多位专家就BR方案联合ASCT的探索展开讨论。孙莹教授认为,BR方案对无法耐受大剂量阿糖胞苷的老年患者以及不适合移植的患者而言是一个不错的治疗选择,在适合移植的年轻MCL患者中,含苯达莫司汀的免疫化疗方案或可考虑前移至一线治疗。黄文荣教授表示,有些传统观念认为BR方案会影响干细胞采集,实际上这个观念缺乏相关的循证医学证据。赵东陆教授提出,临床上很多患者对ASCT的接受度较低,基于window-2研究结果,MCL低危患者即使不接受化疗,经利妥昔单抗联合伊布替尼、维奈克拉治疗后也能有较长的PFS,这提示未来减弱化疗或无化疗方案也可能延长患者生存。此外,将Pola等新型药物的治疗线前移也值得期待,同时关注新药的长期不良反应。黄晨教授补充道,BR方案长期应用可能出现白细胞减低,进而引起体液免疫功能减弱,增加患者的感染风险,因此需对患者进行密切监测。
群英荟·第1期 | 文献精读之初治DLBCL的诊疗新思维
群英荟·第2期 | 文献精读之聚焦惰性淋巴瘤的治疗
群英荟·第3期 | 文献精读之利妥昔单抗难治性iNHL的治疗新进展
群英荟·第4期 | 文献精读之复发难治DLBCL的治疗新进展
群英荟·第5期 | 文献精读之聚焦CLL的治疗
参考文献
[1] Liang Wang, Lin-rong Li, Ken H. Young. New agents and regimens for diffuse large B cell lymphoma. J Hematol Oncol 13, 175 (2020).
[2] Villa D, et al. Bendamustine or high-dose cytarabine-based induction with rituximab in transplant-eligible mantle cell lymphoma. Blood Adv. 2022 Apr 19:bloodadvances.2022007371.
编辑:Chole、苏萌
审校:Evelyn
排版:Wenting
执行:moly
版权声明:CosMeDna所有作品(图文、音视频)均由用户自行上传分享,仅供网友学习交流。若您的权利被侵害,请联系删除!
本文链接://www.cosmedna.com/article/817859128.html